Що таке ISO 13485 та ДСТУ ISO 13485?
ISO 13485:2016 «Medical devices – Quality management systems – Requirements for regulatory purposes» – це міжнародний стандарт, що регламентує створення і впровадження систем менеджменту якості на підприємствах, що займаються випуском медичних виробів, техніки і обладнання. Даний стандарт, як правило, застосовується спільно з ISO 9001:2015 і принципами GMP (належної виробничої практики).. Український аналог цього міжнародного стандарту – ДСТУ ISO 13485:2018. Його впровадження – обов’язкова умова роботи на ринку для виробників медичної продукції та необхідна умова для проведення процедури відповідності Технічним Регламентам. Але хоча український ДСТУ ISO 13485:2018 і є аналогом міжнародного ISO 13485:2016, його дія поширюється лише на території України. В інших країнах український стандарт поки не визнаний і, відповідно, не має юридичної сили. Тому якщо компанія орієнтована на зовнішні ринки, то їй має сенс отримувати сертифікат ISO 13485:2016.
Переваги впровадження ISO 13485
Впровадження ISO 13485 або ДСТУ ISO 13485 дає виробникові можливість оцінювати, контролювати і оптимізувати практично всі етапи виробництва медичних виробів. Це, в свою чергу, допомагає виявити і усунути неефективне використання ресурсів компанії, забезпечити дієвий контроль за виробництвом і якістю продукції і, як наслідок, підвищити свій імідж на внутрішньому і міжнародному ринках. Якщо сертифікація по ДСТУ ISO 13485 є обов’язковою умовою для роботи українських виробників медичних виробів, то проходження сертифікації по ISO 13485 – зовсім не обов’язкова процедура. Проходити або не проходити її підприємства вирішують самостійно. Але тим компаніям, які планують працювати на зарубіжних ринках, дану процедуру пройти необхідно. Адже головна перевага впровадження системи управління якістю ISO 13485:2016 – підтвердження того факту, що продукція, що випускається (медичні вироби) повністю відповідає вимогам міжнародного ринку. І саме сертифікат ISO 13485:2016 міжнародного зразка відкриває для українських виробників медичних виробів двері на зарубіжні ринки.
Як впровадити ISO 13485?
Процес впровадження на підприємстві системи менеджменту якості медичних виробів досить трудомісткий і займає чимало часу – іноді до декількох років. Він складається з безлічі етапів – і жоден з них не можна ігнорувати, адже тільки точну відповідність вимогам стандарту ISO 13485:2016 може гарантувати успішне проведення сертифікації. Якщо коротко, основними етапами впровадження стандарту ISO 13485:2016 можна змалювати таку картину:
- Аналіз відповідності роботи компанії вимогам стандарту;
- Опис процесів та розробка необхідних / відсутніх процедур і документів, обумовлених стандартом.;
- Впровадження системи менеджменту якості;
- Проведення внутрішнього аудиту.
Варто відзначити, що якщо у компанії вже є досвід сертифікації по ДСТУ ISO 13485:2018, то отримати сертифікат відповідності ISO 13485:2016 буде трохи простіше.
Як пройти процедуру сертификації по ISO 13485
IMPROVE MEDICAL – акредитований орган сертифікації відповідності згідно ISO 13485:2016 “Medical devices- Quality management system-Requirements for regulatory purposes” та ДСТУ ISO 13485:2018 «Вироби медичні.Система управління якістю. Вимоги до регулювання» . Наша компетенція і кваліфікація наших співробітників підтверджена атестатами, що діють як на території України, так і за її межами.
Якщо Ваша компанія зацікавлена в отриманні Сертифікату відповідності системі якості ДСТУ ISO 13485:2018 та / або ISO 13485:2016, Ви завжди можете звернутися до нас і укласти договори як на проведення попереднього аудиту, так і на проходження процедури сертифікації.
Звертайтеся до нас за телефоном +38 044 355 50 30 або за електронною поштою info@improvemed.com.ua, і наші експерти з радістю допоможуть вам у вашій діяльності.
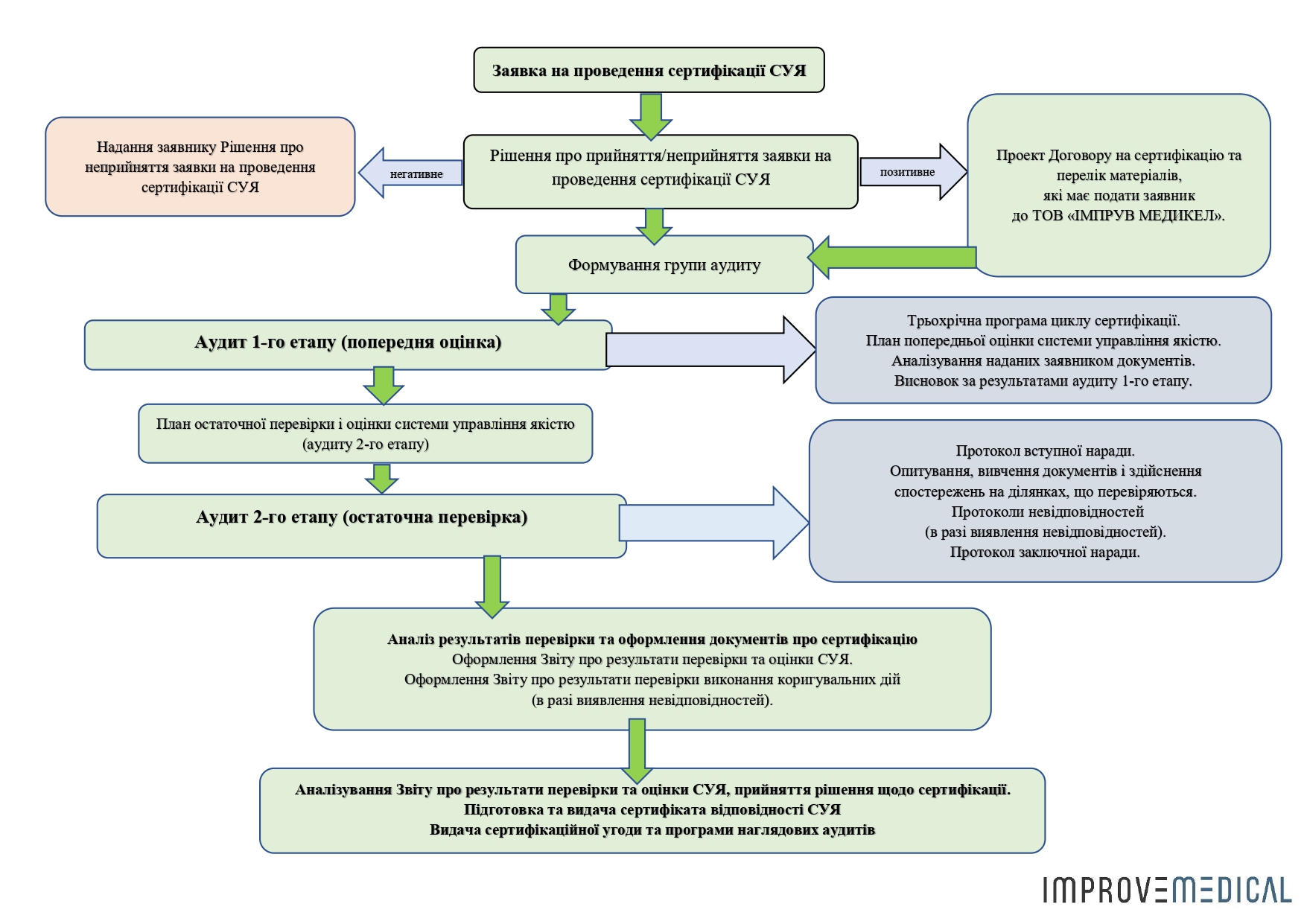
1. Блок-схема сертифікації СУЯ
2. Порядок надання сертифікації та відмови у видачі сертифіката
3. Порядок підтримування сертифікації та повторної сертифікації
4. Порядок призупинення, поновлення та скасування/анулювання сертифікації
5. Порядок скорочення сфери сертифікації
6. Порядок розширення сфери сертифікації